Autores: ALESSANDRIA, Sebastián; GARRIDO, Rosa María.
Recomendaciones Generales
- El plan de tratamiento debe ser decidido en un ateneo multidisciplinario (Comité de tumores) teniendo en cuenta factores predictivos y pronósticos, morbilidad y calidad de vida asociada al tratamiento.
- El tratamiento debe ser realizado por un equipo de profesionales especializado en el diagnóstico y manejo de cánceres ginecológicos.
- Las pacientes deben ser aconsejadas acerca del plan de tratamiento sugerido y las posibles alternativas, incluyendo los riesgos y beneficios de todas las opciones.
Estadificación
- Las pacientes con cáncer de cuello uterino deben estadificarse de acuerdo a la clasificación TNM. La estadificación FIGO (2018) también debe ser documentada. (TABLA 1)
- La clasificación TNM debe basarse en una combinación varias modalidades: examen físico, estudios de imágenes, y anatomía patológica.
- Debe registrarse el método utilizado para determinar el estado del tumor (T), el estado de los ganglios linfáticos (N) y el estado sistémico (M) utilizando las siguientes abreviaturas: clínico (c), por imágenes (I) o por anatomía patológica (p).
Estadificación Clínica y Radiológica
- El examen pélvico y biopsia +/- colposcopía son componentes obligatorios para diagnosticar el cáncer de cérvix.
- El estudio para determinar la extensión del tumor pelviano y para orientar las opciones de tratamiento es la resonancia magnética nuclear pelviana de alta resolución con fase de difusión (RMN). De no contar con los medios se podría realizar una tomografía axial computada con contraste intravenoso.
- La ecografía transvaginal/transrectal es una opción si la realiza un ecografista debidamente capacitado.
- Se puede considerar realizar una cistoscopía o rectoscopía para realizar una biopsia si se documentan lesiones sospechosas en la vejiga o el recto en la resonancia magnética o en la ecografía.
Estadificación Ganglionar y a Distancia
- En el cáncer de cérvix localmente avanzado (T1B2 y superior) o en estadíos tempranos con ganglios linfáticos en imágenes, se recomienda la tomografía por emisión de positrones, tomografía computada (PET-TC) o tomografía computada (TC) de tórax/abdomen para evaluar la enfermedad ganglionar y a distancia.
- El estudio PET-TC es de elección para planificar el tratamiento antes de la quimiorradioterapia con intención curativa.
- Se puede considerar la disección de los ganglios linfáticos paraaórticos, al menos hasta la arteria mesentérica inferior, en el cáncer de cérvix localmente avanzado con ganglios linfáticos paraaórticos negativos en los estudios por imágenes con fines de estadificación. (Evidencia C).
- Se debe considerar realizar una biopsia en caso de sospecha de enfermedad extrauterina para confirmar o descartar enfermedad metastásica y para evitar un tratamiento inadecuado. La biopsia con TRU-CUT es preferible a la biopsia por aspiración con aguja fina, ya que permite la evaluación histológica del tejido.
Ganglios Linfáticos Pelvianos Positivos en la Estadificación Radiológica
- En pacientes con ganglios linfáticos pélvicos inequívocamente comprometidos en las imágenes, se recomienda quimirradioterapia definitiva (QRTc), se puede considerar la disección de los ganglios linfáticos paraaórticos, al menos hasta la arteria mesentérica inferior, en el cáncer de cérvix localmente avanzado con ganglios linfáticos paraaórticos negativos en los estudios por imágenes con fines de estadificación. (Evidencia C).
- Se puede considerar la resección de ganglios linfáticos pelvianos sospechosos.
Medidas Generales
- Historia clínica detallada.
- Biopsia de cuello uterino o revisión de tacos en consulta.
- Rutina de sangre completa, con función hepática y renal. Evaluar serología para HIV.
- Estudio por imágenes.
- Asesoramiento para abandonar el tabaquismo.
- Considerar examinen bajo anestesia
- Citoscopía y rectosigmoideoscopía (≥ Estadío IB3)
Estadificación FIGO 2018
|
IA1 |
Invasión < 3mm |
|
IA2 |
Invasión > 3mm - < 5mm |
|
IB1 |
Tumor > 5 mm - < 2 cm |
|
IB2 |
Tumor > 2 cm - < 4 cm |
|
IB3 |
Tumor > 4 cm |
|
IIA1 |
Compromiso tercio superior de vagina + tumor < 4 cm |
|
IIA2 |
Compromiso tercio superior de vagina + tumor > 4 cm |
|
IIB |
Compromiso del parametrio sin llegar a la pared pelviana, uni o bilateral |
|
IIIA |
Compromiso tercio inferior de vagina |
|
IIIB |
Compromiso del parametrio hasta la pared pelviana, uni o bilateral |
|
IIIC |
1- Metástasis ganglios pelvianos 2- Metástasis ganglios paraaorticos |
|
IVA |
Compromiso mucosa vesical o rectal |
|
IVB |
Órganos a distancia |
Tratamiento IB3- IIA2
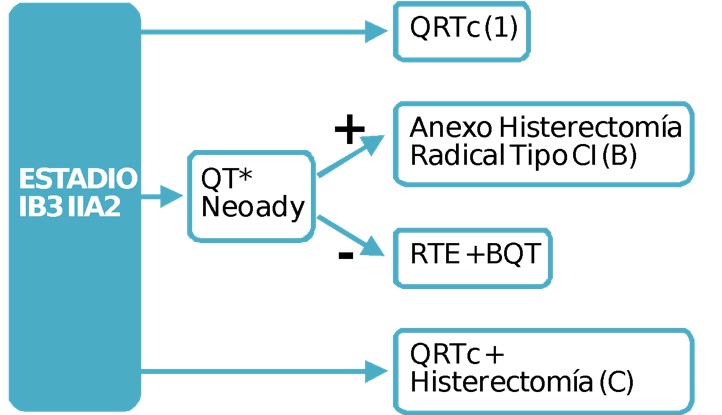
* En tres ensayos aleatorizados de fase III se observo una leve ventaja en SG para la terapia de base de cisplatino administrada de manera simultánea con radioterapia. (Rose PG J Clin Oncol 26 (35): 5802-12, 2008.)
Las complicaciones fueron más altas en las pacientes que recibieron radioterapia adyuvante después de la cirugía.
Manejo del Cáncer de Cérvix Localmente Avanzado
Estadio T1B2 T1B3/T2A1 Y T2A2 y ganglios negativos en la estadificación radiológica
- La estrategia del tratamiento debe tener como objetivo evitar la combinación de cirugía radical y radioterapia externa (RTE) postoperatoria, debido al aumento significativo de la morbilidad y ningún impacto evidente sobre la supervivencia.
- La quimiorradioterapia basada en platino (QRTc) y la braquiterapia (BQT) definitiva son el tratamiento de elección.
- Se puede considerar la disección de los ganglios linfáticos paraaórticos, al menos hasta la arteria mesentérica inferior, antes de la quimirradioterapia y la braquiterapia. la disección de los ganglios linfáticos pelvianos no es necesaria (evidencia c).
- La cirugía radical es una opción alternativa, en particular en pacientes sin factores de riesgo (combinación de 2 o más factores como tamaño tumoral, invasión linfovascular, invasión estromal profunda). Sin embargo, la calidad de la cirugía, tanto la resección de parametrios como la disección de ganglios linfáticos, son de gran importancia en el tratamiento de tumores grandes. se recomienda la evaluación intraoperatoria de los ganglios linfáticos como primer paso. Si en la cirugía se detecta afectación ganglionar, micro o macrometástasis, se debe abandonar la disección adicional de los ganglios pelvianos y la histerectomía radical, y las pacientes deben derivarse para quimiorradioterapia y braquiterapia definitivas. Se debe considerar la disección de los ganglios linfáticos paraaórticos, al menos hasta la arteria mesentérica inferior, con fines de estadificación. Si la evaluación intraoperatoria de los ganglios linfáticos es negativa o no se realiza, se debe realizar una disección sistemática de los ganglios linfáticos pelvianos. se recomienda la histerectomía radical tipo C2.
- La quimioterapia neoadyuvante (QT Neoad) seguida de cirugía radical es una alternativa controvertida. aunque la quimioterapia neoadyuvante ha sido utilizada en regiones donde la radioterapia no está disponible, los datos no sugieren una ventaja en la sobrevida cuando se compara con la cirugía sola en estadios tempranos.
- No se ha demostrado beneficio de la reducción del tamaño tumoral con respecto al pronóstico (Evidencia C).
Estadio T1B2 T1B3/T2A1 Y T2A2 y ganglios comprometidos en la estadificación radiológica
- Se recomienda quimiorradioterapia y braquiterapia definitivas en pacientes con ganglios linfáticos pelvianos inequívocamente afectos en los estudios de imágenes. (Evidencia a)
- Se debe aplicar un refuerzo de radiación adicional a los ganglios linfáticos comprometidos (Evidencia c).
- Se debe considerar la disección de los ganglios linfáticos paraaórticos, al menos hasta la arteria mesentérica inferior, antes del tratamiento para la estadificación en pacientes con ganglios linfáticos paraaórticos negativos en los estudios por imágenes (Evidencia c).
- Se puede considerar la extirpación de los ganglios pelvianos sospechosos.
Tratamiento
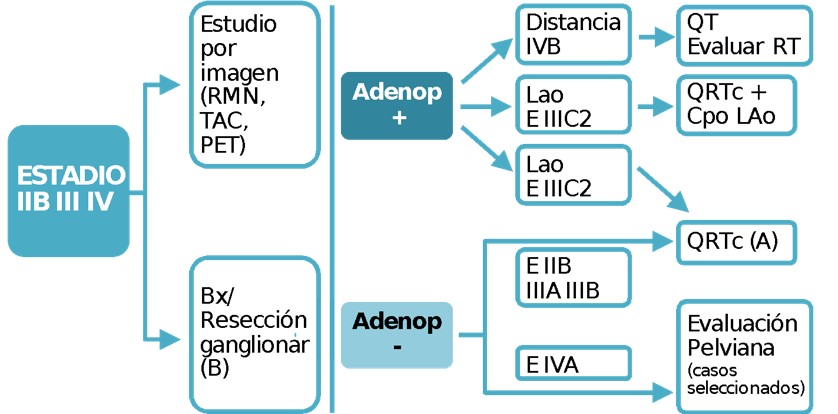
Estadios IIB, IIIA, IIIB, IIIC, IVA
- Se recomienda quimiorradioterapia y braquiterapia definitivas. (Evidencia A)
- Se debe aplicar un refuerzo de radiación adicional a los ganglios linfáticos comprometidos (Evidencia C).
- Se debe considerar la disección de los ganglios linfáticos paraaórticos, al menos hasta la arteria mesentérica inferior, antes del tratamiento para la estadificación en pacientes con ganglios linfáticos paraaórticos negativos en los estudios por imágenes (Evidencia C).
- Se puede considerar la extirpación de los ganglios pelvianos sospechosos. la exenteración pelviana es una opción en casos seleccionados con enfermedad estadío T4.
Cáncer del muñón cervical
- El manejo del cáncer de muñón cervical sigue las recomendaciones para pacientes sin histerectomía subtotal previa. La adaptación de la radioterapia puede ser necesaria, en particular la braquiterapia.
Tratamiento Estadio IVB
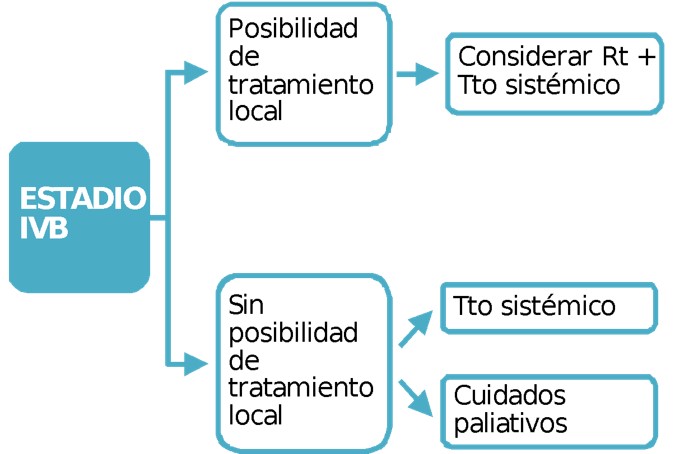
Enfermedad Metastásica a Distancia en la Presentación
- En las pacientes con enfermedad metastásica a distancia en el momento de la presentación se recomienda realizar un estudio diagnóstico completo para evaluar la extensión de la enfermedad, la posibilidad de un tratamiento activo y el tipo de tratamiento, incluido tratamiento de soporte y cuidados paliativos.
- La quimioterapia está recomendada para pacientes con metástasis extrapélvicas que no son candidatas para radioterapia o cirugía de exenteración.
- Si la paciente recibió cisplatino como agente radiosensibilizante, la terapia combinada con platino se prefiere a los agentes únicos en base a numerosos estudios randomizados de fase III. la respuesta a la quimioterapia en estos casos es frecuentemente de corta duración y la sobrevida raramente logra incrementarse.
- En pacientes aptos con enfermedad metastásica diseminada a distancia en la presentación (visceral+/- ganglionar), se recomienda la quimioterapia combinada. carboplatino más paclitaxel o cisplatino más paclitaxel son los esquemas de elección de primera línea. un estudio reciente randomizado fase III (JCOG0505) demostró que el esquema de paclitaxel más carboplatino no es inferior a paclitaxel más cisplatino y se asocia a menor toxicidad en cáncer recurrente o metastásico.
- Se recomienda el agregado de bevacizumab a la quimioterapia estándar en pacientes con buen status funcional. el riesgo significativo de toxicidad gastrointestinal/genitourinaria debe ser evaluado cuidadosamente y discutido con la paciente. los esquemas con bevacizumab han demostrado una ventaja en la sobrevida libre de progresión demostrada en el estudio GOG 240 y en el estudio JGO0505 (recomendación categoría 1).
- El agregado de Pembrolizumab a la quimioterapia con o sin bevacizumab provee una mejora en Sobrevida libre de progresión y Sobrevida global clínicamente y estadísticamente significativa en mujeres con cáncer de cérvix recurrente, persistente o metastásico (Estudio Keynote 826) (recomendación categoría 1). Pembrolizumab + quimioterapia con o sin bevacizumab en 2022 se convirtió en el nuevo estándar de tratamiento para pacientes con cáncer de cérvix persistente, recurrente o metastásico.
Segunda Línea
No hay un esquema estándar en segunda línea. Se sugiere usar monodrogas sobre combinaciones ya que ninguna combinación demostró́ mejoría en la sobrevida, o la participación en estudios de investigación.
Las pacientes con estadio IVB deben recibir tratamiento locoregional, previo o posterior al tratamiento sistémico, en función del caso clínico.
- El algoritmo de tratamiento también puede incluir citoreducción quirúrgica de ganglios linfáticos aumentados de tamaño y quimioterapia adicional.
- En las pacientes con ganglio linfático supraclavicular como único sitio de enfermedad a distancia puede considerarse quimiorradioterapia con intención curativa. el algoritmo de tratamiento debe incluir quimioterapia adicional.
- El papel de la radioterapia para paliar síntomas, como sangrado y dolor, debe considerarse especialmente en pacientes sin tratamiento previo con radioterapia.
Tratamiento de la Recidiva
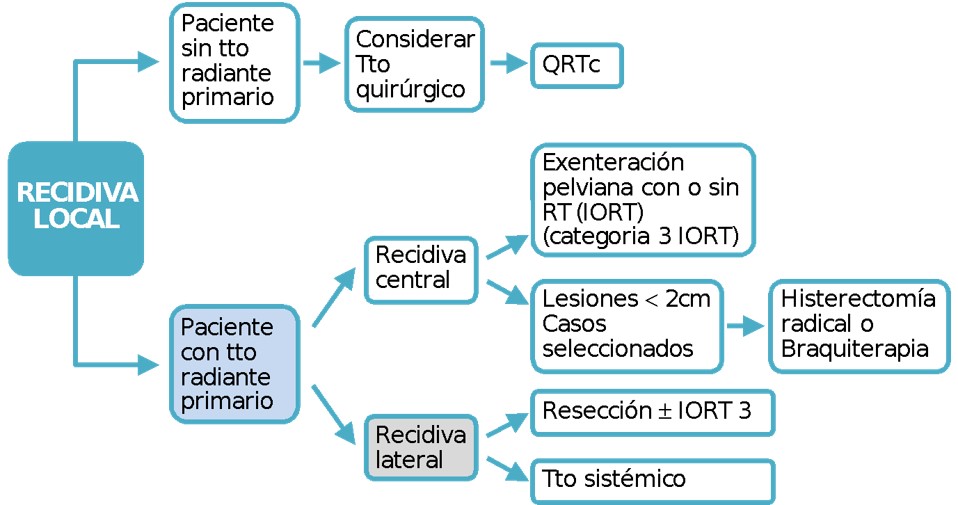
Recidiva
Tratamiento con intención curativa
- En primera instancia confirmación histológica de recidiva.
- Segundo punto excluir las metástasis a distancia, estudios de imagen para establecer el estado de la enfermedad a nivel local, regional y sistémico.
- Es necesaria la conformación de un equipo multidisciplinar que incluye al ginecólogo oncólogo, radioncólogo, radiólogo, patólogo, oncólogo médico, urólogo y cirujano plástico. un programa estructurado para el diagnóstico, tratamiento y seguimiento multidisciplinario.
- Cada centro involucrado en el tratamiento primario del cáncer debe tener un esquema organizado para la discusión de casos complejos y la posibilidad de derivar a pacientes con recidiva para el tratamiento a unidades altamente especializadas.
- Se recomienda la participación en ensayos clínicos para mejorar la evidencia clínica del efecto del tratamiento curativo de la enfermedad recurrente.
- Definir si la paciente es candidata para tratamiento curativo. no se consideran para esta opción las pacientes con metástasis ganglionares/a distancia o enfermedad local multifocal con afectación extensa de la pared pelviana.
- Evaluación del tratamiento primario realizado y de la morbilidad del tratamiento planeado. aconsejar cuidadosamente sobre las opciones de tratamiento, los riesgos y consecuencias que conllevan.
- Las pacientes con una recidiva localizada luego del tratamiento inicial pueden ser candidatas a un retratamiento radical, las opciones incluyen:
- RT y / o quimioterapia; o
- cirugía. en algunas situaciones se han informado tasas de supervivencia a largo plazo de aproximadamente el 40%.
Recidiva Pelviana Central Tras Cirugía Primaria
La quimiorradioterapia definitiva combinada con braquiterapia adaptativa guiada por imagen es el tratamiento de elección. no se recomienda el boost de radioterapia externa, con el objetivo de reemplazar la braquiterapia. (Nivel de evidencia D)
En las pequeñas lesiones superficiales (<5 mm de grosor) en la vagina se pueden tratar usando un colpostato vaginal, mientras que otras lesiones generalmente requieren técnicas intracavitarias intersticiales combinadas.
Recidiva Lateral Posterior a Cirugía Primaria
La quimiorradioterapia definitiva es la opción de elección. (Nivel de evidencia D)
En pacientes altamente seleccionadas y cuando el tumor no invada extensamente la pared lateral de la pelvis, puede ser candidata a exenteración lateral extendida. En los casos en los cuales no se pueden obtener márgenes quirúrgicos libres de lesión se puede combinar radioterapia intraoperatoria. (Evidencia D)
Recidiva Pelviana Central o en Pared Pélvica Lateral Tras Radioterapia o Quimioradioterapia
Si la recidiva es central, y no hay compromiso ganglionar puede ser candidata a una exenteración pelviana, la mortalidad quirúrgica es generalmente del 5% o menor, con tasas de supervivencia cercanas al 50% en pacientes cuidadosamente seleccionados. Si presenta compromiso lateral o afecta la pared pelviana sin compromiso ganglionar en casos muy seleccionados se puede considerar la exenteración lateralmente extendida.
La reirradiación con braquiterapia adaptativa guiada por imagen para recidivas centrales es una opción alternativa, especialmente en pacientes no aptas o que rechazan la cirugía de exenteración, que debe restringirse a centros altamente especializados.
Recurrencias Ganglionares y Oligo Metastásicas
Las recidivas paraaórticos, mediastínicas y/o supraclaviculares localizadas sobre los campos previamente irradiados se pueden tratar con radioterapia externa radical, idealmente en combinación con quimioterapia concomitante. se recomienda irradiar de forma electiva los niveles ganglionares regionales inmediatos por debajo y por encima.
No está claro el efecto terapéutico de la extirpación de la recidiva ganglionar, de ser posible, siempre debe ir seguido de radioterapia.
El manejo de metástasis aisladas en órganos (pulmón, hígado, etc.) debe discutirse en una ateneo multidisciplinar del equipo involucrado en el tratamiento del órgano específico afectado y debe tratarse de acuerdo con el
Método de elección para ese órgano, de acuerdo con el tamaño y la posición anatómica incluyendo resección local, ablación por radiofrecuencia, braquiterapia o radioterapia ablativa estereotáxica.
Tratamiento Paliativo
Las recomendaciones para el tratamiento paliativo sólo deben realizarse después de una revisión completa y minuciosa del caso por un equipo multidisciplinario. en pacientes sintomáticas, el tratamiento paliativo debe adaptarse a la situación clínica.
Se debe tomar en cuenta el estado funcional, comorbilidades, síntomas y deseos de la paciente. Considerar el manejo sintomático. Para controlar el sangrado, el flujo y el dolor debido a enfermedad pelviana o metástasis óseas, la radioterapia paliativa (boost) (evidencia d). en caso de enfermedad sintomática obstructiva o fistulas considerar colostomia, nefrostomias o colocación de stents doble j.
En caso de compresión de la médula espinal debido a metástasis óseas, considerar la intervención neuroquirúrgica o boost de radioterapia.
El sangrado profuso ocurre hasta en el 10% de los pacientes con cáncer avanzado. el tratamiento debe individualizarse y depende de varios factores, incluidas las causas, la probabilidad de revertir o controlar la etiología y la relación costo-beneficio del tratamiento, todo en el contexto de la situación del paciente; carga general de enfermedad, expectativa de vida y objetivos del tratamiento. Si la expectativa de vida de la paciente y la calidad de vida general lo justifican, el tratamiento de un episodio hemorrágico agudo consiste en medidas generales de reanimación, como reposición de volumen y líquidos, y medidas específicas para detener el sangrado. Por otro lado, si los objetivos de la atención del paciente son paliativos, entonces el manejo puede incluir medidas para detener el sangrado sin medidas de reanimación completas. Modalidades locales, como agentes hemostáticos y apósitos, radioterapia, ligadura y coagulación endoscópicas y arterias transcutáneas. embolización, se revisan en el contexto del cáncer avanzado, al igual que los tratamientos sistémicos como vitamina k, vasopresina / desmopresina, octreótido / somatostatina, agentes antifibrinolíticos.
Packing, agentes hemostáticos y apósitos el taponamiento se puede utilizar con o sin presión y puede recubrirse con productos químicos que faciliten la hemostasia. son beneficiosos para el uso tópico exterior en pacientes con cáncer avanzado.
El ácido tranexámico (TA) es un agente antifibrinolítico sintético, el resultado final es una disminución de la lisis de los coágulos de fibrina. se han administrado por vía oral e intravenosa. la dosis intravenosa sugerida de TA es de 10 mg / kg de tres a cuatro veces al día, infundida durante aproximadamente 1 hora. Los efectos adversos más frecuentes son de naturaleza gastrointestinal (náuseas, vómitos y diarrea) y se producen en el 25% de los casos los efectos adversos parecen depender de la dosis. la tromboembolia es infrecuente. Estos antifibriolíticos también se pueden aplicar por vía tópica o rectal. Una revisión sistemática de ensayos aleatorizados encontró que los medicamentos hemostáticos. Carecen de grandes estudios controlados de estos fármacos en el ámbito del cáncer. Sin embargo, la evidencia que respalda esto se basa en gran medida en informes de casos.
Seguimiento
Se recomienda la educación del paciente con respecto a los síntomas que sugieren una recurrencia (flujo vaginal; pérdida de peso; anorexia; dolor en la pelvis, caderas, espalda o miembros inferiores; tos persistente). Los pacientes también deben recibir asesoramiento sobre tener un estilo de vida saludable, obesidad, nutrición, ejercicio, salud sexual (utilización de dilatadores vaginales, lubricantes en especial en pacientes que recibieron RT), abandonar el habito de fumar, terapia de reemplazo hormonal y posibles efectos a largo plazo y tardíos del tratamiento.
Se sugiere realizar el seguimiento con un equipo con experiencia. se recomienda la anamnesis y el examen físico cada 3 a 6 meses durante 2 años, cada 6 a 12 meses durante otros 3 hasta cumplir los 5 años de finalizado el tratamiento efectivo y luego anualmente. A pesar que la tasa de detección de cáncer de cuello uterino recurrente es baja utilizando solo la citología cervical y vaginal, anualmente debe realizarse.
Los estudios por imágenes recomendados, el PET/CT (preferida), la TAC o RMN deben realizarse entre de los 3 a 6 meses posteriores a la finalización del tratamiento. basándose en la sintomatología, hallazgos anormales en el examen físico o nuevos síntomas pelvianos, abdominales o pulmonares.
Otras pruebas son opcionales según las indicaciones clínicas, como el hemograma completo semestral, el nitrógeno ureico en sangre (BUN) y las determinaciones de creatinina sérica.
Pacientes con enfermedad persistente o recurrente pueden ser evaluados quirúrgicamente en casos seleccionados, seguida de terapia para la recaída.
Las pacientes que fueron portadoras de cáncer de cuello uterino tienen mayor riesgo de padecer segundos cánceres, sumado a que las pacientes que incluyen como parte de su tratamiento a la RT tienen riesgo de padecer segundos cánceres inducidos por radiación, especialmente en sitios irradiados cerca del cuello uterino (colon, recto, ano y/o vejiga).
Cáncer de Cérvix en el Embarazo
Es la neoplasia maligna ginecológica que se diagnostica con mayor frecuencia en mujeres embarazadas.
Ante una paciente a la que se le diagnostica cáncer de cuello durante el embarazo un dilema clínico y requiere atención multidisciplinaria en ginecológica oncología, neonatología, obstetricia, anestesiología, radioterapia, oncología clínica, psicología y de ser necesario conformar un comité de ética. El tratamiento debe ser consensuado e individual en relación con la intención de la paciente, el estadio del tumor y la edad gestacional del embarazo en el momento del diagnóstico del cáncer. Las mujeres deben tomar la difícil decisión de retrasar el tratamiento hasta la madurez fetal documentada o someterse a un tratamiento inmediato según su estadio los objetivos principales del plan de tratamiento recomendado son la seguridad oncológica de la mujer embarazada y sin morbilidad adicional al feto.
El tratamiento de las pacientes con cáncer de cuello en el embarazo debe realizarse exclusivamente en las instituciones que cuenten con servicios de ginecológica, oncología y perinatología con experiencia en todos los aspectos del tratamiento oncológico, del embarazo y la atención de los neonatos prematuros.
El compromiso de los ganglios sospechosos debe verificarse histológicamente debido a su importancia pronóstica y al impacto en el manejo hasta la semana 24 de la gestación (viabilidad fetal mínima), preferiblemente por abordaje mínimamente invasivo.
Dependiendo del estadio y la edad gestacional del embarazo, las opciones de tratamiento, deben discutirse con el paciente considerando los riesgos y beneficios:
- Quimiorradioterapia concurrente definitiva según lo recomendado para el estadio de la enfermedad sin preservación del embarazo, con o sin terminación previa del embarazo. (evidencia D)
- Retraso del tratamiento oncológico hasta la madurez fetal (si es posible >32 semanas de gestación) y comienzo del tratamiento específico para el cáncer inmediatamente después del parto por cesárea. (evidencia D)
- Quimioterapia neoadyuvante hasta alcanzar la madurez fetal y el comienzo del tratamiento específico del cáncer inmediatamente después del parto por cesárea. el tratamiento después del parto debe considerar la aplicación de quimioterapia previa. en pacientes con estadio localmente avanzado o con tumor residual después de la conización que no puede extirparse por completo (riesgo de rotura prematura de membranas y/o insuficiencia cervical), se puede considerar la quimioterapia basada en platino comenzando no antes de las 14 semanas de gestación. (evidencia D).
- La vía de finalización del embarazo recomendada es la cesárea después de la 32 semana de gestación (si es posible). El parto espontáneo tiene un impacto pronóstico negativo en estas pacientes. En el momento de la cesárea o después de ella, se debe realizar un tratamiento oncológico ajustado al estadio definitivo correspondiente al de las mujeres no embarazadas teniendo en cuenta la terapia que ya se ha administrado durante el embarazo.
Tablas Adyuvancia
Carcinoma Escamoso, Adenocarcinoma, O Carcinoma Adenoescamoso
|
Quimioradiación |
Enfermedad recurrente o metastásica |
||
|
CISPLATINO |
Primera línea esquema combinado |
Primera línea agentes únicos |
2da línea |
|
CARBOPLATINO si la paciente tiene intolerancia a cisplatino. |
Otros esquemas recomendados
|
Otros esquemas recomendados
|
|
|
ENFERMEDAD RECURRENTE O METASTÁSICA |
|
Terapia De Segunda Línea Esquemas De Primera Elección Pembrolizumab para tumores PDL-1 positivos.
|
|
OTROS ESQUEMAS RECOMENDADOS
|
Diagnóstico por Imágenes Inicial
(Tabla 1)
- Resonancia magnética nuclear con contraste para evaluar la extensión local de la enfermedad (recomendada sobre todo en estadíos figo IB2 y IB3).
- Tomografía de tórax sin contraste.
- PET/TC (recomendada) o TC con contraste de tórax, abdomen y pelvis en estadíos figo mayor o igual a IB1.
- En pacientes con hallazgo incidental de cáncer de cérvix en histerectomía total se recomienda -PET/TC o TC con contraste de tórax, abdomen y pelvis para evaluar presencia de enfermedad metastásica y RMN de pelvis con contraste para evaluar enfermedad pelviana residual.
Bibliografía Tratamiento Sistémico
- Colombo N, Dubot C, Lorusso D, et al. KEYNOTE-826 Investigators. Pembrolizumab for Persistent, Recurrent, or Metastatic Cervical Cancer. N Engl J Med. 2021 Nov 11;385(20):1856-1867.
- Tewari KS, Sill MW, Long HJ, et al. Improved survival with Bevacizumab in advanced cervical cáncer. N Engl J Med 2014 Feb 20; 370:734-743.
- Monk BJ, Sill MW, McMeekin DS, et al. Phase III trial of four cisplatin containing doublet combinations in stage IVb, recurrent, or persistent cervical carcinoma: a Gynecologic Oncology Group Study. J ClinOncol 2009; 27:4649-4655.
- 3-Moore DH, Blessing JA, McQuellon RP, et al. Phase III study of cisplatin with or without paclitaxel in stage IVb, recurrent or persistent squamous cell carcinoma of the cérvix: a Gynecologic Oncology Group Study. J ClinOncol 2004; 22: 3113-3119.
- Moore KN, Herzog TJ, Lewin S, et al.A comparison of cisplatin/paclitaxel and carboplatin/paclitaxel in stage IVb, recurrent or persistent cervical cáncer.Gynecol Oncology 2007; 105: 299-303.
- Kitagawa R, Katsumata N, Shibata T, et al. Paclitaxel plus carboplatin versus paclitaxel plus cisplatin in metastatic or recurrent cervical cáncer: the open-label randomized phase III trial JCOG0505. J ClinOncol 2015; 33: 2129-2135.
- Long HG, Bundy BN, Grendys EC, et al. Randomized phase III trial of cisplatin with or without topotecan in carcinoma of the uterine cervix. A Gynecologic Oncology Group Study. J ClinOncol 2005; 23: 4626-4633.
- Marabelle A, Le DT, Ascierto PA, et al. Efficacy of pembrolizumab in patients with noncolorectal high microsatellite instability/mismatch repair-deficient cancer: results from the phase 2 KEYNOTE-158 study. J ClinOncol 2020;38:1-10.
- Woodruff R. Haematological problems. In: Woodruff R, ed. Palliative Medicine: Symptomatic and Supportive Care for Patients with Advanced Cancer and AIDS. Melbourne, Australia: AperulaPty Ltd., 1993:228-252.
- Dean A, Tuffin P. Fibrinolytic inhibitors for cancer-associated bleeding problems. J Pain Symptom Manage 1997;13:20-24.
- Lorusso D, Petrelli F, Coinu A, et al. A systematic review comparing cisplatin and carboplatin plus paclitaxel-based chemotherapy for recurrent or metastatic cervical cancer.Gynecol Oncology 2014; 133: 117-123.
- Chung HC, Ros W, Delord JP, Perets R, Italiano A, Shapira-Frommer R, Manzuk L, Piha-Paul SA, Xu L, Zeigenfuss S, Pruitt SK, Leary A. Efficacy and Safety of Pembrolizumab in PreviouslyTreatedAdvanced Cervical Cancer: ResultsFromthePhase II KEYNOTE-158 Study. J ClinOncol. 2019 Jun 10;37(17):1470-1478.
- Frenel JS, Le Tourneau C, O'Neil B, Ott PA, Piha-Paul SA, Gomez-Roca C, van Brummelen EMJ, Rugo HS, Thomas S, Saraf S, Rangwala R, Varga A. Safety and Efficacy of Pembrolizumab in Advanced, ProgrammedDeathLigand 1-Positive Cervical Cancer: ResultsFromthePhaseIb KEYNOTE-028 Trial. J ClinOncol. 2017 Dec 20;35(36):4035-4041.